1928년 4월 6일, 미국의 생물학자 제임스 왓슨 (James Dewey Watson, 1928 ~ 2025) 출생
제임스 듀이 왓슨 (James Dewey Watson, 1928년 4월 6일 ~ 2025년 11월 6일)은 미국의 분자 생물학자, 유전학자, 동물학자로, 1953년 프랜시스 크릭과 함께 DNA의 이중 나선 구조를 발견한 것으로 잘 알려져 있다.
이 업적으로 1962년 노벨 생리의학상을 수상했다.

– 제임스 듀이 왓슨 (James Dewey Watson)
.출생: 1928년 4월 6일, 미국 일리노이주 시카고
.사망: 2025년 11월 6일 (97세)
.성별: 남성
.국적: 미국
.학력: 시카고 대학교 학사, 인디애나 대학교 석사
.경력: 하버드 대학교 생물학과 교수
.직업: 분자 생물학자, 유전학자, 동물학자
.활동 기간: 1953년 ~ 2025년
.소속: 하버드 대학교
.상훈: 노벨 생리학·의학상 (1962)
그는 시카고 대학교 학사 후에 인디애나 대학교에서 석사 학위를 취득했고, 영국 케임브리지 대학교의 캐번디시 연구소에서 연구했다.
여기서 그는 미래의 공동연구자인 프랜시스 크릭을 처음으로 만나게 된다.
DNA의 구조 규명 이후 미국의 하버드 대학교 생물학과 교수로 분자생물학 연구를 해오고 있다.
게놈 프로젝트를 주창했고 이 프로젝트의 초대 책임자를 맡기도 했다.
저서로는 교과서인 The Molecular Biology of the Gene (1965), DNA구조 발견에 대한 베스트 셀러인 The Double Helix (1968)가 있다.
그는 인종주의적으로 인식될 수 있는 여러 논쟁적인 발언 때문에 구설수에 오르고 있기도 하다.
왓슨은 2025년 11월 6일에 별세했다. 향년 97세

○ 생애 및 활동
왓슨은 1928년 4월 6일 미국 일리노이주의 시카고에서 태어났다. 그는 원래 살바도르 루리아의 작업을 통해 분자 생물학을 시작하게 되었다. 루리아는 유전자 돌연변이에 관한 ‘루리아 델브룩 실험’으로 유명한 생물학자이다. 루리아는 세균을 감염시키는 박테리오파지를 사용가능하게 하는 연구원 단체에 속해 있었다. 루리아와 막스 델브뤽은 초파리와 같은 유전적 제도에서 세균 유전학으로 움직이려는 유전학자들의 중요한 운동인 새로운 “파지 그룹”(Phage Group)의 리더였다. 1948년 초 왓슨은 인디아나 대학의 루리아의 실험실에서 그의 박사 과정을 시작했다. 그 해 봄, 그는 루리아의 아파트에서 델브뤽을 처음 만났고, 그 해 여름 왓슨의 Cold Spring Harbor Laboratory 로의 첫번째 이동에서 또 그를 만나게 되었다.
왓슨은 파지 그룹을 매개로 하여 과학자로써 일하였는데, 본래 파지 그룹의 멤버들은 자신들이 유전자의 실체적 본질의 발견으로 나아가고 있다고 생각했다. 1949년 왓슨은 펠릭스 하우로위즈와 같이 당시의 전통적 관점인 유전자가 단백질이고 스스로 복제할 수 있다는 내용을 담고 있는 강의를 받았다. 염색체의 다른 중요한 분자 요소인 DNA는 “멍청한 테트라뉴클레오티드” (stupid tetranucleotide)라고 받아들여졌었다. 그러나 이런 이른 시기에도 파지 그룹의 영향을 받고 있는 왓슨은 DNA가 유전 물질이라고 제안한 에이버리-맥클라우드-맥카트 실험을 알고 있었다. 왓슨의 연구 프로젝트는 엑스레이를 이용해 박테리아 바이러스를 불활성화 시키는 내용을 담고 있었다. 1950년 그는 22세의 나이로 인디애나 대학에서 그의 동물학 박사 학위를 받았다.
왓슨은 1950년 9월, 박사 후 연구를 위해 생화학자 코펜하겐 대학의 허번 칼크라의 실험실로 처음 향했다. 칼크라는 효소의 핵산 합성에 관심이 있었고 그는 파지를 실험적 제도로 이용하길 원했다. 그러나 왓슨은 DNA 구조에 대해 알고 싶어 했기에 그의 관심은 칼크라의 것과는 일치하지 않았다. 칼크라와 그 해에 일을 한 후에 왓슨은 파지 그룹의 일원으로 활동하는 대신 미생물학적 물리학자인 올리 말로에와 실험을 하기 위해 나머지 시간을 코펜하겐에서 썼다.
왓슨이 지난 여름의 콜드스피링하버 phage 학회에서 배웠던 실험은 파지의 어떤 분자 요소가 실제로 타겟 세균을 감염시키는지를 알아낼 수 있는 추적자로써의 방사성 인산염을 사용하는 법을 담고 있었다. 그 목적은 단백질과 DNA 중 유전 물질이 무엇인지 알아내는 것이었지만 델브뤽의 자문에 의하면 그들은 그들의 결과가 결정적이지 않다는 것을 알아내었고 그 결과는 DNA로 새롭게 이름 붙여진 분자를 정확하게 알아볼 수 없었다. 왓슨은 절대 칼크라와의 건설적인 상호교류를 하진 않았으나 이탈리아에서의 미팅에서는 동행했다. 이곳에서 왓슨은 모리스 윌킨스가 자신의 DNA 엑스레이의 회절 데이터에 대해 말하는 것을 보았다. 왓슨은 당시 DNA가 더 자세하게 설명될 수 있다고 확신을 가졌다.
1951년, 캘리포니아의 화학자 라이너스 폴링은 분자 모델 구성과 엑스레이 결정학에서의 그의 노력의 산물인 알파 나선 아미노산 모델을 출판했다. 그의 파지와 인디애나 대학, Statens Serum Institute (덴마크), Cold Spring Harbor Laboratory와 캘리포니아 공과대학에서의 다른 실험으로부터 어느 정도의 결과를 얻고 난 후, 왓슨은 DNA구조를 알아낼 수 있게 해주는 엑스레이 회절 실험을 배우고 싶다는 욕구를 갖게 되었다. 그 해 여름, 루리아는 존 켄드루를 만났고 그는 잉글랜드의 왓슨을 위해 새로운 박사후 연구 프로젝트를 마련했다.
왓슨과 크릭은 처음엔 DNA가 삼중나선일 것이라 생각했기에 3가닥 모형을 만들었지만 염기들의 수소결합을 암시하는 노팅엄대학 매슨 걸랜드 연구팀의 DNA의 산성도에 따른 점성도의 변화 실험을 뒤늦게 알게되어 이중나선구조를 고려하게 되었다. 이후 폴링의 잘못된 가설의 논문을 들고 윌킨스와 플랭클린에게 보여주려고 떠난 여행에서 윌킨스가 플랭클린이 최근에 찍은 X선 회절 사진을 왓슨에게 보여줘 DNA가 이중나선이라는 사실을 확신하게 되었다.

1953년 3월, 왓슨과 프랜시스 크릭은 DNA의 이중나선 구조를 추정했다. 왓슨과 크릭이 일하는 캐번디시 실험실의 감독인 로렌스 브래그 경(Sir Lawrence Bragg)은 1953년 4월 8일, 솔베이 컨퍼런스에서 벨기에에서 발견한 단백질을 처음 발표했다. 하지만 그것은 인쇄되지는 않았다. 왓슨과 크릭은 1953년 4월 25일 출간된 과학저널 <네이처>에 논문을 제출했다. 이것은 다른 생물학자들과 노벨상 수상자들로부터 20세기에서 가장 중요한 과학적 발견으로 불리게 된다. 브래그는 런던의 Guys Hospital Medical School에서 1953년 5월 14일 목요일에 The News Chornicle of London지의 1953년 5월 15일자의 리체 캘더의 논문 “Why You Are You. Nearer Secret of Life”에서 나온 결과에 대해 강연했다.
시드니 브래너, 잭 두니츠, 도로시 호드킨, 리슬리 오겔과 베릴 오톤(Beryl M. Oughton)은 옥스퍼드 대학의 화학과에서 일하던 1953년 4월 왓슨과 크릭의 DNA 모델을 처음 봤던 사람들이었다. 모두가 그 새로운 DNA 모델에 감명받았는데 특히 케임브리지의 캐번디시 연구소와 새로운 분자생물학 연구소에서 그 후에 크릭과 일하게 된 브래너가 그랬다. 케임브리지 대학의 학생 신문인 Varsity도 1953년 5월 30일 그 신문만의 짧은 기사를 실었다.
왓슨은 1953년 6월 초 제 18회 Cold Sring Harbor Symposium on Viruses에서 DNA 이중나선에 대한 논문을 발표했다. 왓슨과 크릭이 네이처에 논문을 실은지 6주 후였는데, 그 모임의 많은 사람들은 아직 그 발견에 대해 듣지 못했었다. 1953년 Cold Harbor Symposium 은 많은 사람들이 DNA 이중나선 모델을 처음으로 볼 기회였다. 왓슨, 크릭 그리고 윌킨스는 1962년 그들의 핵산의 구조에 대한 연구로 노벨 생리학·의학상을 받았다.
하버드 대학에서 왓슨은 1956년에 시작해 조교수로부터, 부교수, 정교수로 연속 승진을 달성했다. 그는 하버드대의 초점에 있어서, 생태학, 발생 생물학, 분류학, 생리학 같은 훈련들이 침체되어 왔고 그런 것들은 분자 생물학의 기초가 되는 훈련일 뿐이고 생화학은 그들의 기초를 밝혀왔다는 진술을 통해 고전 생물학에서 분자 생물학으로 바꾸는 것을 옹호했다. 그는 심지어 학생들이 그들의 연구가 방해한다고 주장하기도 했고, 1976년에 학교를 떠났다.
1968년, 왓슨은 Cold Spring Harbor 연구소의 감독이 되었다.1968년 3월 28일 왓슨은 캘리포니아 주 샌디에고의 라홀라 해변의 교회에서 엘리자베스 루이스와 결혼했다. 1970년과 1972년 사이에 왓슨은 두 아들을 갖게 되었고, 1974년 그의 가족은 Cold Spring Harbor에 그들의 보금자리를 만들었다. 왓슨은 35년과 연구 감독과 연구 소장으로써 일했고 나중에 대학 총장의 역할까지 맡게 되었다. 그곳에서의 그의 과거의 업적에 대해 말하자면, 연구소장 브루스 스틸번은 “짐 왓슨은 어떤 과학계에도 비할 바 없는 연구 환경을 만들어냈다”며, “그의 감독 하에 그 연구소는 암의 유전적 기본에 대한 이해를 통해 중요한 공헌을 만들어내게 되었다”고 진술했다. 일반적으로, 감독, 연구소장, 그리고 총장으로서의 왓슨은 CSHL을 오늘날의 임무를 “암과 신경학적인 질병과 다른 인간 고통의 원인을 이해하는 것을 발전시키기 위한 분자 생물학과 유전학의 탐구에의 기여”로 만들었다. 2007년 1월, 왓슨은 Champalimaud Foundation의 장인 레너 블레자의 권유를 받아들여 재단의 고문을 하는 기관인 과학적 심의회의 장이 되었다.
2007년 10월, 언론에 그의 인종주의적 발언이 노출되어 큰 논란을 일으켰다. 결국 왓슨은 인종과 지능에 관한 비판적 관점을 철회했고, 1주 후인 25일에 79세의 나이로 “40년 가까이 고귀한 봉사를 했던” Cold Spring Harbor 연구소에서 은퇴했다. 왓슨은 성명서에서 그의 은퇴 이유를 그의 나이와 주변 환경으로 설명했다.
이외에도 왓슨은 Chang Yi Wang이 설립한 Board of Directors of United Biomedical의 이전 멤버였다. 그는 6년간 일하고 1999년 은퇴했었다. 왓슨은 또한 Allen Institute for Brain Science의 이전 고문이었다. 앨런 연구소는 자선가 폴 앨런과 조디 앨런에 의해 2003년에 만들어진 시애틀과 워싱턴에 있는 비영리 의학 연구 단체이다. 신경과학자들의 많은 전문 단체, 분자 생물학자들, 정보학자들, 공학자들, 수학자들, 통계학자들 그리고 수치적 생물학자들이 앨런 연구소의 과학적 중심을 이루기 위해 불러들여졌다. 생쥐 모델 시스템을 이용하여 각 분야의 과학자들이 성숙한 생쥐의 20000개의 유전자의 발현과 세포수준을 넘어 신경해부학적 경계에서 유전자 발현 지도를 그리기 위해 모였다. 이런 접합의 노력으로부터 얻어진 데이터는 Allen Mouse Brain Atlas에서 공개되어 있으며, 이를 통해 뇌의 신경적인 회로와 그 기능을 정의하는 신경해부학적 기본을 넘어 추가적인 문제를 추구할 수 있다.
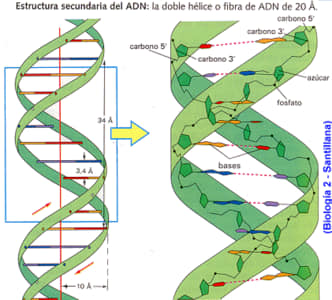
– 업적 : 이중나선구조
왓슨과 크릭은 DNA가 뉴클레오타이드로 구성된 이중나선 구조라고 설명하였다. 만일 DNA 이중나선을 꼬여진 사다리로 생각한다면 발판은 수소결합으로 연결된 A-T와 G-C염기쌍이고, DNA의 가로대는 공유결합으로 연결된 디옥시리보오스와 인산이 교대로 배열되어 있다. DNA 뉴클레오티드에는 디옥시리보오스, 염기, 인산이 각각 하나씩 있다. DNA는 흔히 직선 구조로 묘사되지만 실제로는 아주 복잡하고 그 복잡성이 DNA 기능에 도움이 된다. DNA 뉴클레오티드에 포함된 염기는 아데닌, 구아닌, 시토신, 티민이다. 아데닌과 구아닌은 2개의 유기 고리 구조를 갖는 퓨린이고, 시토신과 티민은 1개의 유기 고리 구조를 갖는 피리미딘이다. A와 T 그리고 G와 C가 수소결합으로 연결된 염기쌍은 각 염기쌍이 하나의 고리 구조와 2개의 고리 구조를 갖기 때문에 나선 사이의 거리가 일정하다. 이러한 퓨린-피리미딘 쌍을 상보적 염기쌍 (complementary base pair) 또는 염기쌍이라 부른다. 상보적 염기쌍은 유전자 기능과 DNA 복제의 기본이다.
DNA 이중 나선을 구성하는 두개의 사슬은 서로 반대방향으로 달리고 있는데 이러한 머리-꼬리 배열은 DNA가 역평행임을 의미한다. 화학 규칙에 따라 디옥시리보오스의 탄소에 오른쪽에서 왼쪽으로 차례대로 번호를 붙이면 분명해진다. DNA 가닥은 디옥시리보오스의 5번 탄소에서 시작하여 3번 탄소에서 끝이 난다. 두 가닥은 서로 반대방향으로 놓여있다. 하나의 완전한 나선의 회전은 10 개의 염기쌍인 34Å의 길이에 해당한다. 각 염기쌍은 3.4Å에 해당하며 가닥들이 교차하는 지역에서는 관찰자에게 수직인 염기쌍들이 숨겨져 있다. 내경은 10Å이고 외경은 20Å이다. 이중나선의 원통형의 윤곽은 크고 작은 두 개의 고랑을 가지며 모두다 폴리펩티드 사슬을 수용할 정도로 충분히 크다. 아데닌-티민 (A-T) 염기쌍은 두 개의 수소결합을 가지는 반면, 구아닌-시토신 (G-C) 염기쌍은 세 개의 수소결합을 가진다.
엄청난 양의 DNA가 간단한 세포 안에 채워져 있는데, 만일 인간의 염색체 46개에 있는 DNA 염기를 A,C,T,G로 표기하면 32억 개의 문자가 차지하는 분량은 500쪽 책 4,000권에 해당된다. 세포는 DNA를 실패에 감듯이 히스톤 단백질을 이용하여 체계화 시킨다. 진핵세포에서 하나의 염색체를 형성하기 위하여, 146개의 염기쌍이 8개의 히스톤 (histone) 단백질로 이루어진 구조물 주위를 두 번 휘감아 1개의 뉴클레오솜 (nucleosome)을 형성한다. 뉴클레오솜의 지름은 10nm이다. 연속적인 DNA는 실에 꿰인 구슬처럼 뉴클레오솜을 연결하고, 이것이 다시 접혀 지름 30nm의 구조물을 형성한다. 이러한 DNA 응축 방법은 분열하는 세포에서 고도로 응축된 중기 염색체를 만든다. 분열하는 세포는 DNA 응축 정도를 달리하면서 필요한 부분에 효소가 접근할 수 있도록 허용한다. DNA가 부분 부분이 풀리면서 RNA로 전사된다. 전사를 하기 위하여 DNA가 히스톤에서 떨어져 나오거나 단단히 감겨있어도 DNA 본래의 구조와 염기 서열은 그대로 유지된다. 마찬가지로, 세균과 고균의 DNA도 단백질과 함께 응축되어 있다.

– 암과의 전쟁
이중나선을 발견한 뒤 왓슨은 영국을 떠나 미국으로 돌아왔다. 그는 캘텍에 잠시 머무른 다음 1956년에 하버드 대학 생물학 교수로 부임했다. 1962년 노벨상 수상은 생물학자로서 그의 삶에 세계적인 명성을 안겨주었다. 하지만 정작 하버드에서 왓슨은 순조롭게 적응하지 못했다. 그는 하버드에서의 교수 생활 대신에 뉴욕주 롱아일랜드 북부 해변에 위치한 콜드 스피링 하버 연구소를 이끌어나가는 연구관리자 일에 매력을 느꼈다. 19세기 말에 생물학자들의 여름철 휴양을 겸한 실험연구소 용도로 세워진 콜드 스프링 하버 연구소는 특히 멘델 유전학의 수용에 앞장서면서 미국 유전학의 발전에 기여하기 시작했다.
1940년대에는 파지유전학자들의 요람 역할을 톡톡히 수행하기도 했지만, 1960년대에 들어서는 그 규모와 비전에서 쇠퇴한 모습을 드러내기도 했다. 과거 이곳을 본거지로 삼았던 파지그룹의 한 사람이기도 한 왓슨은 일찍부터 콜드스프링 하버 연구소의 청사진을 그려나가고 있었다. 시간제로 하버드와 콜드 스프링 하버를 오가며 근부하던 왓슨은 1968년 끝내 하버드의 교수직을 정리하고 콜드 스프링 하버의 연구소장직에 전념했다. 소장으로서 그의 청사진은 연구소를 세계적 분자생물학 연구센터로 거듭나게 하는 것이었다. 왓슨은 분자생물학 혁명의 목적이 우리 삶의 질을 향상시키는 데 있다고 보았다. 그는 유전자 치료와 암 정복에 대한 도전을 연구소의 모토로 삼았다.
1911년에 미국의 프랜시스 라우스가 후대에 라우스육종바이러스라 불리는 발암 바이러스를 발견해 1966년에 노벨 생리의학상을 수상하는 등, 암의 원인 규명과 정복에 대한 관심과 경쟁이 일었다. 왓슨은 연구소의 새로운 일을 바로 분자생물학과 유전학의 측면에서의 암 연구에서 찾았다. 연구소장으로서 그의 궁극적인 목표는 콜드 스프링 하버 연구소를 세계 최고의 암 연구센터로 키워내는 것이었다.
1971년 12월 닉슨 미국 대통령은 국가암퇴치법을 통과시켜 역사상 최대의 암 정복 운동을 벌였다. 법안의 요지는 연방정부가 국립암연구소를 통해 암 정복의 기초 연구에 엄청난 규모의 연구기금을 10여 년에 걸쳐 지원한다는 것이었다.
그동안 생명 메커니즘을 이해하기 위한 DNA 연구가 꾸준히 이루어져온 결과, 1960년대 말에는 분자유전학, 바이러스학, 동물세포 배양 기술 등이 고등동물세포 내에서의 생화학적 연구를 혁명적으로 변모시켰다.
예를 들어 포유류와 인간의 세포를 마치 박테리아의 경우처럼 배양접시에서 성장시킬 수 있는 획기적인 방법론이 개발되었다. 또한 종양바이러스로 알려진 일부 동물바이러스는 배양세포를 암세포로 변화시키는 기능이 있음이 보고되었다. 이러한 노하우를 응용해 세균배양용 샬레에서 암세포를 키워 악성종양의 기원과 진행에 대한 통제된 실험을 수행하는 것이 가능해졌다. 이로부터 실험실에서의 암 연구는 새로운 호기를 맞게 되었다.
1958년 이후 콜드 스프링 하버 연구소는 동물세포와 그 바이러스를 배양하는 새로운 기법을 소개할 수 있는 여름학술프로그램의 개발에 주력했다. 또한 이전의 파지 생물학자들에게는 암 기초 연구에 전념하게 함으로써 종양바이러스 모델의 개발에만 마음을 쓰게 했다. 박테리오파지가 박테리아세포의 유전학을 증명하는 수단을 제공했듯이, 이제 종양바이러스는 포유동물 세포에 비슷한 방법으로 접근할 수 있게 만들었다.
왓슨은 분자바이러스학이 암의 신비를 밝혀내는 핵심열쇠라고 믿었다. 그는 규모도 작고 전망도 없어 보였던 이 연구소의 소장으로 부임하자마자 후원자를 찾아 나섰다. 1968년 미국국립보건원의 지원하에 동물바이러스와 종양바이러스에 대한 과제 수행에 나섰다. 왓슨의 지도에 따라 연구소의 재원은 엄청나게 늘어났다. 과학 지도자로서 왓슨의 능력은 돋보였다. 특히 연구소가 나아갈 과학 어젠다 (agenda)의 설정과 인물을 바라보는 통찰력이 두드러졌다.

왓슨은 콜드 스프링 하버를 최상의 암 연구소로 도약시키고자 했다. 암을 일으키는 바이러스는 DNA와 RNA 종양바이러스 두 가지로 분류되는데, DNA 종양바이러스는 세포를 암 변형시키는 서열, 즉 암유전자를 가지고 있어 세포나 동물에 감염되면 암을 발생시킬 수 있었다. 종양바이러스 연구프로그램을 구축하려한 왓슨은 당시 널리 알려진 종양바이러스인 SV40 (Simian vacuolating virus 40) DNA 연구로 유명한 젊은 바이러스학자 조지프 샘브룩을 연구소로 초빙했다. 그리하여 샘브룩을 중심으로 종양바이러스 그룹이 연구소에 설치되었다.
1970년 의학계와 정치권의 관심에 힘입어 암 정복이라는 국가적 과제가 수면 위로 떠오르자, 콜드 스프링 하버는 이러한 준비 덕에 그 수혜자가 될 수 있었다. 1972년에는 5년 동안의 암 연구기금을 국립암연구소로부터 유치하면서 샘브룩은 최고 수준의 젊은 종양바이러스학자들을 연구소로 끌어들여 연구 역량을 한층 강화했다.
콜드 스프링 하버의 연구자들은 1970년대에 선보인 제한효소 기술을 신속하게 채택했다. 또한 그들은 분자 수준의 DNA와 RNA 분석에 필요한 제한효소 사용 기술을 개발하는 데 주력했다. 그들은 강력한 새 분석도구인 에티듐 브로마이드 아가로오스 겔 (ethidum bromide agarose gel)로 크기가 다른 DNA분자를 분리할 수 있는 값싸고 신속한 방법을 개발했다.
이러한 기법은 제한효소에 의해 잘려진 바이러스 DNA의 단편을 분리하는 데 효과적인 방법임이 입증되었다. 이 기법은 또한 암세포 변형을 초래한 종양바이러스 DNA의 부위를 알아내고 이러한 변형유전자가 바이러스 염색체상에 존재하는 위치를 파악하는 데도 사용되었다. 배양세포에서 악성종양의 변화를 유도하는 유전자들을 종양유전자라고 부르는데, 콜드 스프링 하버 연구소는 바로 종양유전자에 의해 생성된 단백질을 정제하고 바이러스복제에서의 그 기능을 규명하는 데 초점을 맞추었다.
종양 바이러스 그룹의 초기 연구는 바이러스 DNA가 단백질 합성을 위해 RNA 정보로 전사하는 메커니즘에서 성과를 거두었다. 1977년 연구소의 리처드 로버츠가 RNA 접합절단 또는 분할유전자를 발견한 것이다. 일반적으로 mRNA는 핵 안의 DNA로부터 유전정보를 읽어 단백질 합성이 일어나는 세포질에 유전정보를 전달한다. 정보를 전달하기 전 미성숙 mRNA는 불필요한 염기 서열인 인트론을 제거하고 유용한 염기인 엑손을 연결하는 과정인 접합절단을 거치게 된다. 콜드 스프링 하버의 실험과학자들은 MIT의 연구자들과 함께 RNA 정보는 단백질 합성 이전에 편집된다는 것을 보여주었다. 기능 유전자 내에 띄엄띄엄 있는 것은 단백질 합성을 위해 잘려나간 쓸데없는 DNA 염기였다.
1972년경 로버츠는 수많은 미생물로부터 새로운 제한효소를 정제하는 기술을 개발했다. 1980년경이 되어 세상에 알려진 제한효소의 절반 이상의 그의 실험실에서 분리되었다. 이러한 효소들이 DNA 재조합 관련 업체에 의해 상업적으로 활용될 기미가 보이자, 로버츠는 새롭게 발견된 효소를 무료로 전 세계 학계 연구자들에게 제공했다. 이를 계기로 콜드 스프링 하버는 종양 바이러스 연구자들을 위한 메카가 되었으며, 이 연구소의 소장으로서 암과의 전쟁에 선봉에 선 왓슨은 다시 한 번 세상의 주목을 받게 되었다.
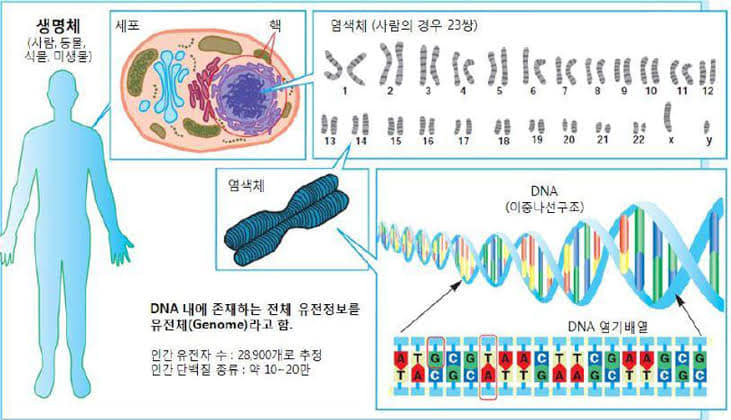
– 인간게놈프로젝트
1988년, 60세의 연륜과 경험이 있는 왓슨은 NIH 산하 인간게놈 연구기획에 합류했고, 그 이듬해에는 인간게놈연구센터의 초대 소장에 임명되었다. 1990년 8월에는 NIH와 DOE 공동으로 HGP가 시작되었다. 미국 연방정부가 산하 기관을 통해 지원하는 이 프로젝트는 인간으로서의 기능을 발휘하게 하는 청사진인 모든 유전정보를 완전히 해독한다는 것이다. 인간 유전체의 염기 서열 전부를 해독하고, 아울러 게놈지도를 가능한 한 정확하게 작성하는 일에도 초점을 맞추는 것이었다. 게놈지도는 유전자 지도와 물리지도로 분류해 연구되었다.
유전자 지도란 염색체 위에 유전 표지판들이 어떤 순서로 놓여 있는지, 즉 각 표지의 상대적인 위치를 파악하는 것이다. 물리지도는 염색체상에 놓여 있는 유전 표지판의 절대적인 위치를 파악하는 것이다. 즉, 유전자 지도 작성은 유전체의 기본 구조를 밝혀내는 것이고, 물리지도 작성은 어느 서열이 정확히 염색체의 어디에 있는지 밝혀내는 것이라고 할 수 있다.
이렇게 염색체에서 각 서열이 있는 정확한 위치를 알면 그것을 기준으로 삼아 다른 서열이 있는 위치도 찾아낼 수 있다. 인간게놈 분석은 2005년도 완성을 목표로 약 15년 동안 연간 2억 달러 정도의 비용이 들것이라고 예상되었다.
HGP에서 왓슨의 역할과 관련해 주목할 것이 있다. 그가 이 프로젝트에 내재한 잠재적 분란에 대한 제도적인 대비책을 마련한 것이다. 그는 HGP 예산의 일부를 이 프로젝트가 일으킬 수 있는 과학적, 윤리적 문제에 대한 연구에 투입하도록 주도했다.
우리는 과거 우생학이 잘못 사용된 예를 잘 살펴보아야 한다. 바로 미국과 독일에서 불완전한 지식이 오만하고 끔찍한 방식으로 사용되었다. 우리는 사람들에게 자신의 DNA가 개인적인 것이며 아무도 그것을 손에 넣을 수 없다는 점을 확신시켜야 한다.
왓슨의 선언에 힘입어 HGP가 본격화된 1990년부터 게놈연구의 윤리적, 법적, 사회적 의미를 연구하는 프로젝트 ‘윤리, 법, 사회관계’에 연간 예산의 5%가 투입되었다. HGP에서의 띠냐 연구는 HGP로부터 예상되는 문제점 도출과 그에 대한 실제적인 제도적 대안 마련, 교육 프로그램의 개발 등 다양한 활동을 폈으며, 이후 ELSI 연구는 생명공학 프로젝트 등에서 필수적인 세부 과제로 점차 자리잡게 되었다.

또한 왓슨이 이끄는 HGP는 양적으로도 상당한 지원을 확보할 수 있었다. 한 의학잡지는 이렇게 적었다.
“왓슨의 매력은 과학적으로 무지한 의원들을 충동하고 현혹하는 데 더없이 중요한 마법의 요소를 가지고 있다. 이 저명한 ‘이중나선’의 저자는 그들의 마음을 쉽게 사로잡았다.”
안타깝게도 1992년 HGP가 본궤도에 오르기 시작할 무렵 왓슨은 NIH의 소장으로 붕미한 버너딘 힐리와 충돌을 빚으면서 HGP 일선에서 물러났다. 두 사람의 분쟁 원인은 DNA의 특허 문제 때문이었다. 왓슨은 NIH의 연구자들이 분석한 수천 건의 DNA 서열을 가지고 정부 특허 취득에 나서겠다고 한 힐리의 결정을 비판하고 나섰다. 힐리는 유전체 덩어리에 특허권을 얹어 상업적 가능성을 얻어 정부의 이익을 보호하고자 했다. 하지만 왓슨은 불확실한 유전자에 특허를 내줄 경우 장기적으로 유전자를 이용한 의학 연구와 발전은 끔찍하리만큼 지체될 것이라고 보았다. 특허 문제에 대한 공개논쟁이 종료되면서 왓슨은 HGP를 떠났다.
1992년을 기점으로 HGP는 국제적인 양상을 띠게 되었다. 프로젝트를 미국이 주도하고 분석 작업 역시 절반 이상이 미국에서 이루어졌지만, 영국, 프랑스, 독일, 일본을 비롯한 쟁쟁한 국가들이 이 프로젝트에 추가로 동참했다. HGP는 전 세계18개국의 연구진이 참여하는 국제 컨소시엄으로 발전했다. 예를 들어 인간 이외에도 세균에서 꼬마선충에 이르기까지 몇 가지 생물의 염기 서열 분석이 완료되는 등 그 범위와 속도를 더하게 되었다.
무엇보다도 HGP 연구 성과에 탄력을 준 일은 1998년 미국의 민간 생명공학회사인 셀레라 지노믹스 사가 인간 유전체 연구에 뛰어들면서 HGP와 경쟁구도를 형성하게 된 것이다. 이에 유전자 해독 작업은 급류를 타기 시작하여 2005년까지 끝내기로 한 것을 2003년으로 앞당겨 끝냈다. 2000년 6월에는 HGP 컨소시엄과 셀레라 지노믹스 사가 공동으로 인간게놈지도 초안을 완성하여 발표했다. 마침내 수정된 목표보다 2년여가 더 빠른 2001년 2월에 이 두 조직은 전체 인간게놈지도를 완성했다고 공식적으로 발표했다. 이에 따라 생명현상에 대한 좀더 확실한 접근이 가능해지고, 인류가 시달려왔던 많은 유전병 치료와 의약용으로 쓰일 각종 생체물질의 연구와 생산이 가능하게 됐다.
인간게놈지도가 완성됨으로써 암과 심장병 같은 복잡한 유전병에 대해 얻게 될 생물학적 통찰력은 물론 의학적 혜택 또한 엄청나다. 이는 각종 인간 질병의 예방과 치료 등 의학 분야에 혁명을 가져올 것이다. 또한 인간의 생명현상을 이해하는 기초가 될 위대한 업적으로 평가된다. 이로써 의학과 건강, 인류의 복지에서 혁명적 진전이 가능할 것이다. 이미 반세기 전 DNA 이중나선 구조의 발견으로 생명현상의 신비를 규명하는 데 가장 강력한 불씨를 지핀 주인공의 하나인 왓슨은, 약 반세기가 지난 지금, 다시 인류복리를 위한 응용을 목적으로 HGP라는 거대한 도전에도 뛰어들었다.

– 논란의 발언들
왓슨은 종종 유전자 연구 영역 내에서 논란거리가 될만한 발언을 하거나 다른 사람을 반박하곤 했다. 왓슨은 ‘멍청함’을 질환이라고 얘기하며, ‘정말 멍청한’ 하위 10%의 사람들은 치료를 받아야 한다고 말했다. 또한 그는 사람의 ‘미모’는 유전자 조작을 통해 조작할 수 있다고 제안했다. 왓슨은 “사람들은 모든 여자가 예쁘게 되면 끔찍할 것이라고 말하지만, 난 그 편이 좋을 것 같다”라고 말했다. 왓슨이 “만약 어떤 여자가 동성애적 성향을 가진 아이를 원치 않고, 우리가 성적 취향에 관여하는 유전자를 찾을 수 있다면 우리는 그 여자의 결정을 존중해야 한다”라고 말한 것이 Sunday Telegraph에 인용되었다. 이에 대해 생물학자 리처드 도킨스는 “잡지에서 왓슨의 말을 왜곡했고, 왓슨은 낙태를 찬성하는 입장을 표명한 것이 아니라 단지 그런 부모의 결정을 존중해야할 필요성도 있다라고 말하는 것이다”라고 말했다.
왓슨은 “당신은 뚱뚱한 사람을 면접을 보게 되면 그 사람을 고용하지 않을 것을 알기 때문에 기분이 나쁘다”라는 비만에 대해 논란거리가 될 만한 발언을 했다. 2000년 컨퍼런스에서 왓슨은 피부 색깔과 성욕 사이의 관계에 대해 발표했다. 그리고 그는 비키니를 입은 여자의 사진을 슬라이드에 띄우면서, 멜라닌이 성 충동을 향상시킨다고 말했다. 그 후 그는 “이것이 당신에게 라틴계 연인이 있는 이유입니다.”라는 발언을 해서 논란이 되었다.
또한 왓슨은, 2007년 영국 선데이타임스와의 인터뷰에서 “흑인들이 백인과 동일한 지적 능력을 갖췄다는 전제 하에 이뤄지고 있는 서구 국가들의 아프리카 관련 정책들은 잘못됐다”며 “인종간 지능의 우열을 가리는 유전자가 앞으로 10년 안에 발견될 수 있을 것”이라고 말해 파문을 일으켰다. 당시 그는 문제가 커지자 지난 18일 보도자료를 통해 “벌어진 일들에 대해 당혹감을 느낀다”며 공식 사과했지만 영국에서는 왓슨 박사의 발언을 놓고 논란이 계속됐다. 인간 게놈 지도 제작을 이끈 크레이그 벤터 박사는“피부색과 지능간의 상관관계가 있다는 과학적 근거는 물론 그런 유전 정보도 없다”며 왓슨 박사의 발언에 대해 유감을 표했고 켄 리빙스턴 런던 시장은“근거없는 인종주의 이론이 유전공학을 악용해 인종간 우열 순위를 매기려 한다”며 왓슨 박사의 발언을 과학의 탈을 쓴 인종주의적 선전문구라고 비난했다. 이로 인해 영국 각지에서 다양한 행사에 참석할 예정이었지만 CSHL이 왓슨 박사에 대해 직무정지 결정을 내린 이후 왓슨 박사를 초청하기로 했던 기관들이 줄줄이 일정을 취소하는 사태가 벌어졌다.
그러나 영국 의학연구협의회 회장인 옥스퍼드대학의 콜린 블레이크모어 교수는 “왓슨 박사가 도발적이고 정치적으로 편향돼 있다는 점은 널리 알려져 있지만 그런 뛰어난 과학자가 자신의 불쾌한 견해로 인해 침묵을 강요당한다는 것은 불행한 일”이라는 의견을 보였고 리처드 도킨스 옥스퍼드대 석좌교수 또한 왓슨 박사에게 있을 오류는 과학적 논쟁을 통해 규명돼야 한다고 말했다.

○ Awards and honors
Albert Lasker Award for Basic Medical Research, 1960
Benjamin Franklin Medal for Distinguished Achievement in the Sciences (2001)
Copley Medal of the Royal Society, 1993
CSHL Double Helix Medal Honoree, 2008
Eli Lilly Award in Biological Chemistry, 1960
EMBO Membership in 1985
Gairdner Foundation International Award, 2002
Honorary Member of Royal Irish Academy, 2005
Honorary Fellow, the Hastings Center, an independent bioethics research institution
Honorary Knight Commander of the Order of the British Empire (KBE), 2002
Irish America Hall of Fame, inducted March 2011
John J. Carty Award in molecular biology from the National Academy of Sciences
Liberty Medal, 2000
Lomonosov Gold Medal, 1994
Lotos Club Medal of Merit, 2004
National Medal of Science, 1997
Nobel Prize in Physiology or Medicine, 1962
Othmer Gold Medal (2005)
Presidential Medal of Freedom, 1977
Golden Plate Award of the American Academy of Achievement, 1986
– Honorary degrees received
DSc, University of Chicago, US, 1961
DSc, Indiana University, US, 1963
LLD, University of Notre Dame, US, 1965
DSc, Long Island University (CW Post), US, 1970
DSc, Adelphi University, US, 1972
DSc, Brandeis University, US, 1973
DSc, Albert Einstein College of Medicine, US, 1974
DSc, Hofstra University, US, 1976
DSc, Harvard University, US, 1978
DSc, Rockefeller University, US, 1980
DSc, Clarkson College of Technology, US, 1981
DSc, SUNY at Farmingdale, US, 1983
MD, Buenos Aires, Argentina, 1986
DSc, Rutgers University, US, 1988
DSc, Bard College, US, 1991
DSc, University of Stellenbosch, South Africa, 1993
DSc, Fairfield University, US, 1993
DSc, University of Cambridge, United Kingdom, 1993
DrHC, Charles University in Prague, Czech Republic, 1998
ScD, University of Dublin, Ireland, 2001
– Professional and honorary affiliations
American Academy of Arts and Sciences
American Association for Cancer Research
American Philosophical Society
American Society of Biological Chemists
Athenaeum Club, London, member
Cambridge University, Honorary Fellow, Clare College, Cambridge
Cold Spring Harbor Laboratory, Chancellor Emeritus; Honorary Trustee; Oliver R. Grace Professor Emeritus (all revoked in 2019)
European Molecular Biology Organization, member since 1985
National Academy of Sciences
Oxford University, Newton-Abraham Visiting Professor
Royal Danish Academy of Sciences and Letters
Royal Society, Foreign Member of the Royal Society (ForMemRS) since 1981
Russian Academy of Sciences

○ 저서
The Double Helix (1968년): 이중 나선 – 핵산의 구조를 밝히기까지, 하두봉 옮김, 전파과학사, 2000
Avoid Boring People (And Other Lessons from a Life in Science) (2008년): 지루한 사람과 어울리지 마라, 김명남 옮김, 이레
Passion for DNA (2000년): DNA를 향한 열정, 이한음 옮김, 사이언스북스
DNA – The Secret of Life (2003년): DNA – 생명의 비밀, 이한길 옮김, 까치글방
– Selected books published
James D. Watson, The Annotated and Illustrated Double Helix, edited by Alexander Gann and Jan Witkowski (2012) Simon & Schuster, ISBN 978-1-4767-1549-0.
Watson, J. D. (1968). The Double Helix: A Personal Account of the Discovery of the Structure of DNA. New York: Atheneum.
Watson, J. D. (1981). Gunther S. Stent (ed.). The Double Helix: A Personal Account of the Discovery of the Structure of DNA. W. W. Norton & Company. ISBN 0-393-95075-1. (Norton Critical Editions, 1981).
Watson, J. D.; Baker, T. A.; Bell, S. P.; Gann, A.; Levine, M.; Losick, R. (2003). Molecular Biology of the Gene (5th ed.). New York: Benjamin Cummings. ISBN 0-8053-4635-X.
Watson, J. D. (2002). Genes, Girls, and Gamow: After the Double Helix. New York: Random House. ISBN 0-375-41283-2. OCLC 47716375.
Watson, J. D.; Berry, A. (2003). DNA: The Secret of Life. New York: Random House. ISBN 0-375-41546-7.
Watson, J.D. (2007). Avoid Boring People and Other Lessons from a Life in Science. New York: Random House. p. 366. ISBN 978-0-375-41284-4.



참고 = 위키백과
크라스천라이프 편집부
